Молчание РНК как заслон от аллергии
Успешное считывание гена на матричную РНК вовсе не означает, что кодируемый им белок будет построен: эта мРНК может быть разрушена в цитоплазме клетки. Такое явление, названное посттранскрипционным молчанием, часто наблюдается при внесении дополнительных генов в ДНК растений. Впервые оно было описано еще в 1990 г., когда при введении в геном петунии дополнительных копий гена, отвечающего за красную окраску цветков, количество красного пигмента не только не возросло, но и значительно снизилось (Napoli et al., 1990).

Механизм «замолкания РНК» снижает эффективность работы генных инженеров. С другой стороны, его можно использовать для создания растений, устойчивых к растительным вирусам, так как он может способствовать разрушению не только их собственных матричных РНК, но и соответствующих РНК вирусов, которым удалось проникнуть в клетки растений.
Судя по всему, механизмов посттранскрипционного молчания существует несколько, и ученые пока не вполне понимают, как они работают и как связаны между собой, белые пятна в этой области только начинают заполняться (Плотников, 2007). Есть предположение, что отдельные молекулы мРНК активно деградируют при достижении определенного порога своей численности (Abler, 1996). Другая теория основана на изменениях в регуляции работы генома, связанных с метилированием ДНК, в результате чего среди нормальных РНК синтезируется некоторое количество «ненормальных», которые и запускают распад мРНК в цитоплазме (Hoofvan, 1997).
Одним из хорошо описанных механизмов посттранскрипционного молчания является РНК-интерференция. Этот метод базируется на способности молекул двухцепочечных РНК эффективно подавлять активность сходных с ними по строению генов. В последние годы РНК-интерференцию используют в прикладных исследованиях, направленных на получение нокаутных (содержащих «молчащие» гены) клеток, тканей и организмов. Ведь если грамотно использовать этот механизм, то теоретически можно «выключить» в клетке производство любого белка.
Среди успешных примеров применения этого метода — получение двух сортов кофейного дерева, содержащих в плодах пониженный на 30–50% алкалоид кофеина. Схожий эксперимент был проведен и с табаком с целью понизить в растении содержание никотина (Рябушкина, 2009).

Другая возможность использования этого подхода — подавление синтеза аллергенов. И это уже не сказка: генетикам из испанского Института сельского хозяйства в Кордове почти полностью удалось освободить зерна пшеницы от глиадина — одного из составляющих глютена. Именно из-за глиадина группа запасающих белков пшеницы вызывает у многих людей иммунную реакцию. Правда, и без использования системы редактирования генома CRISPR/Cas9 тут не обошлось (Sanchez-Leon et al., 2017).
Конечно, в этом направлении ученым еще работать и работать, но уже есть надежда, что совсем скоро можно будет смело есть арахисовое масло без боязни умереть от анафилактического шока! Важно отметить, что подобное вмешательство генной инженерии в метаболизм растений отличается от традиционного: в геном не встраивается чужеродный ген, а значит, не происходит и синтеза чужеродного белка. Из-за этого РНК-интерференцию можно назвать генным вмешательством со сниженным экологическим риском
Более того, даже формально такое вмешательство не несет на себе печати «ГМО».
Каков же итог нашей экскурсии по современным методам селекции? Шанс сделать выбор в пользу «натуральных» злаков, овощей и фруктов мы давно упустили. Прогресс, в том числе и в создании новых видов растений, остановить невозможно, но осознавать и правильно оценивать риски распространения и употребления генетически модифицированных продуктов необходимо.
Сегодня, когда общество проявляет большую озабоченность безопасностью пищевых продуктов, селекционеры находятся в ситуации, вынуждающей их использовать альтернативные пути получения новых сортов растений. В силу тех или иных причин эти методы не относятся к запрещенным, но в ряде случаев являются не менее рискованными, чем традиционные методики получения ГМО.
Также не стоит забывать, что грамотный подход к селекции растений с использованием техник редактирования генома позволяет минимизировать использование пестицидов и удобрений — что это означает для экологии, нет нужды объяснять. В любом случае, какие продукты мы будем есть завтра, в огромной степени зависит уже не от природы, а от нас самих.
Публикация подготовлена на основе статьи, которая участвовала в научно-популярном конкурсе «Био/мол/текст»-2017 портала «Биомолекула».
Описание и характеристика сорта
Персик сорта «Харнас» формирует высокорослые и достаточно зимостойкие деревья. Плоды массой до 170-180 г, шарообразной формы, ярко-красного цвета, без опушения. Мякоть желтая, сочная, кисло-сладкого вкуса, легко отделяющаяся от косточки, очень вкусная.
Персики «Harnas» полностью вызревают в последних числах июля или первой декаде августа. Спелые плоды не опадают с деревьев, что можно отнести к неоспоримым преимуществам сорта. Персики данного сорта характеризуются внешней привлекательностью и очень высоко ценятся благодаря товарному виду. Урожай пригоден к транспортировке в течение четырех суток после съема.
Снижаем риски: от ТРАНС к ЦИС и ниже
Сейчас прохождение всех тестов на биобезопасность и вывод на рынок генетически модифицированных организмов, в том числе растений, жестко регулируется на международном уровне. В этом вопросе правовая база ЕС опирается на директиву Европейского парламента и Совета Европейского союза от 12 марта 2001 г. «О преднамеренном выпуске в окружающую среду генетически модифицированных организмов». Примечательно, что данный нормативный документ исключает из перечня ГМО организмы, полученные путем скрещивания, экстракорпорального оплодотворения, полиплоидной индукции, возникновения мутаций и слияния протопластов скрещиваемых видов (соматическая гибридизация).
Законодательство РФ в области ГМО растительного происхождения регулируют 4 федеральных закона и 6 постановлений Правительства РФ, в том числе федеральный закон № 86-ФЗ «О государственном регулировании в области генно-инженерной деятельности» от 5 июля 1996 г. Ожидается вступление в силу постановления, позволяющего узаконить возделывание ГМ-культур на территории России, которые пока можно выращивать только на опытных участках. Для ввоза в нашу страну сегодня разрешены 22 линии пищевых и кормовых ГМ-растений, среди которых кукуруза, картофель, соя, сахарная свекла и рис, а любые ГМО и ГМ-продукты должны проходить обязательную регистрацию.

В свою очередь, мировое ученое сообщество считает, что нужно различать ГМО по способу получения и делать послабления для продуктов, полученных умеренным вмешательством. Так появилась система деления ГМО на три вида: ТРАНС, ЦИС и ИНТРА.
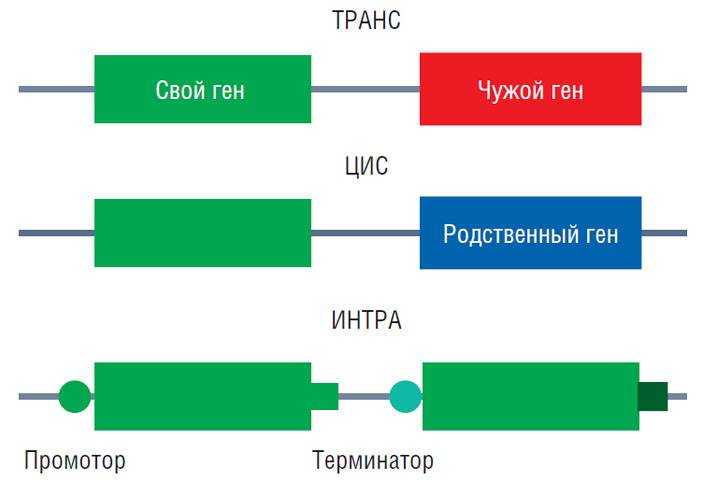
Трансгенными сегодня называют организмы с искусственно введенными генами, которые в принципе не могут быть приобретены путем естественного скрещивания. Это могут быть гены растений других видов или животных, например рис, в геном которого встроен ген кукурузы. Потенциальная опасность трансгенных культур в том, что приобретенные таким образом новые качества могут повлиять на пригодность к использованию в пищевых или кормовых целях, а затем передаться диким родственникам, что может иметь непредсказуемые последствия для природных экосистем
По этой причине законодательные и регулирующие органы развитых стран уделяют большое внимание биобезопасности таких культур, чтобы снизить риск экологических сдвигов

В геном цисгенных растений могут быть введены гены организмов того же или близких видов, с которыми возможно скрещивание в естественных условиях. При этом сам целевой ген не должен быть видоизменен или оторван от своих регуляторных последовательностей. Пример цисгенного растения — картофель, не подверженный картофельной гнили благодаря встраиванию генов диких видов картофеля из Анд, устойчивых к этому заболеванию. Такой картофель сейчас создается в Бельгии (VIB’s fact series, 2015)
Важно, что цисгенезис не привносит в организм растения принципиально новых для него признаков и, по сути, аналогичен традиционному скрещиванию с родственными дикими формами
Интрагенезис можно считать продолжением концепции цисгенезиса, но в этом случае в ДНК растения встраивают его собственный ген, совмещенный с регуляторными участками других его генов. В ходе такой модификации искусственно создаются новые комбинации из уже имеющихся в растении участков ДНК (Holme, 2013). Подобное изменение регуляции активности генов позволяет усиливать полезные признаки (например, способность накапливать витамины в листьях) или, напротив, устранять или сводить к минимуму нежелательные.
Между тем при современном регулировании оборота ГМО-различия между трансгенными и цисгенными растениями не учитываются, хотя эти типы кардинально различаются. Из-за жестких рамок, установленных законодательством, получение и использование цисгенных растений серьезно затруднено, что может заблокировать или значительно отсрочить проведение дальнейших исследований по улучшению сортов сельскохозяйственных культур. Пока лишь в Канаде контроль за цисгенными растениями менее строг по сравнению с трансгенными (Schouten, 2006).
Когда Стива Джобса «попросили» из Apple, он купил Pixar
Все изменилось в 1986 году: Джордж Лукас продал отдел разработки Lucasfilm вместе со всеми ресурсами Стиву Джобсу за $10 млн, по крайней мере, именно так сделка была представлена широкой общественности. В реальности все было несколько сложнее, ведь в то время обе «стороны сделки» были, мягко говоря, не в лучшем положении. Отдел Кэтмелла еще в 1983 году начинает испытывать финансовые трудности, Лукас год за годом срезает финансирование, не видя быстрого успеха инвестиций, а вскоре переживает развод и раздел имущества с бывшей супругой.

Эд Кэтмелл, Стив Джобс и Джон Лассетер. Фото lawrencelevy.com
За два года до этого из-за постоянных скандалов и скверного характера Стива Джобса отстраняют от работы в его собственном детище — Apple. Собравшись с силами, он основывает новую компанию NeXT Computer, серьезно увлекшись будущим компьютерной графики. На одной из многочисленных отраслевых выставок Джобс знакомится с Лукасом, и их планы совпадают. Сразу же после приобретения, 3 февраля 1986 года, в штате Калифорния была зарегистрирована независимая компания Pixar.
«Если бы я знал в 1986 году, чего мне будет стоить сохранить Pixar, я сомневаюсь, что купил бы компанию. Ключевая проблема заключалась в том, что в течение многих лет стоимость компьютеров, необходимых для создания анимации, которую мы могли бы продавать, была чрезвычайно высокой. Это сводило на нет все наши усилия», — объяснял много позже Джобс журналу Fortune.
Всей команде Pixar во главе с Кэтмеллом и Лассетером пришлось немало потрудиться, чтобы перевести Pixar из статуса неликвидного актива в статус перспективного проекта, особенно в глазах нового шефа. Джобс поручил Pixar отложить в сторону мечты об анимации и фильмах, вместо этого сосредоточившись на технической графике для рекламы и короткого метра, которую они могли бы продать. Джобс собирался использовать Pixar для демонстрации возможностей компьютеров NeXT — анимационной рекламы, первое время так и происходило, но дела шли не очень успешно. Компании не удавалось даже окупить собственное содержание, и Джобсу приходилось из своего кармана выписывать чеки на зарплаты сотрудникам. По примерным оценкам, прежде чем получить прибыль, он вложил в Pixar еще около $50 млн…
Эпигенетика: чуть-чуть не считается
Одними из самых молодых и суперсовременных альтернатив для селекционеров стали подходы эпигенетики — науки о наследуемых механизмах управления экспрессией генов (Marjori, 2015). Как работает наш генетический код, общеизвестно, но вот тонкости его надстройки (эпи- означает ‘над’), своего рода «дирижера», управляющего работой генома, во многом остаются загадкой.
Начало производства белков в клетке регулируется множеством факторов. У клетки также имеются приемы, заставляющие «замолчать» тот или иной ген, чтобы предотвратить производство уже ненужного белка: это и разрушение еще незрелых молекул РНК, считанных с генетической «матрицы», и создание «механических» препятствий для самого считывания ДНК (Marjori, 2014). В общем, эпигенетических сигналов в клетке очень много, они не до конца изучены, однако некоторые из них уже используются для селекции растений, которые попадают к нам на стол каждый день.
Подавить работу генов в клетке можно с помощью природного механизма — РНК-зависимого ДНК-метилирования, суть которого состоит в присоединении метильной группы (СН3) к нуклеотиду цитозину, стоящему в определенном положении. В результате блокируется процесс считывания информации с ДНК на молекулу РНК (Zhang, 2013).
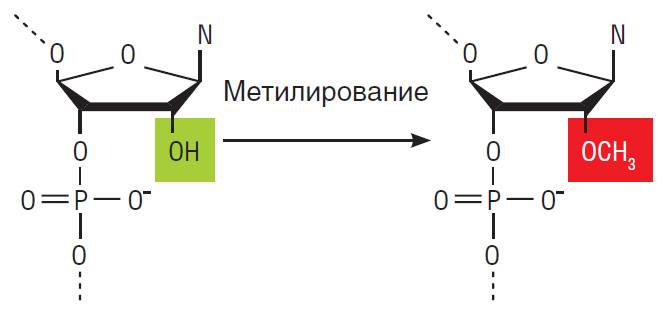
Метилирование ДНК у растений и животных осуществляется ферментами ДНК-метилтрансферазами. Сами по себе эти ферменты метилировать ДНК не могут: им нужны специальные некодирующие РНК, которые направляют метилтрансферазы к конкретным участкам ДНК. Более того, считается, что в метилировании ДНК участвуют еще два вида РНК: малые интерферирующие РНК и микроРНК. Все вместе эти молекулы и определяют, какой именно участок ДНК цепи нужно метилировать. Сегодня такие РНК можно ввести в растение с помощью разных методик, например, посредством вирусов растений или с помощью техник генной инженерии (Deng, 2014).
Интересно, что если ученый изменяет признак растения с помощью ДНК-метилирования и при этом не вносит в геном никаких мутаций, то такое растение не считается ГМО. Если же некодирующие РНК не вводятся извне, а производятся самим растением благодаря геномному редактированию, то оно уже относится к генно-модифицированному.
Но и тут можно схитрить. Дело в том, что у растений метилирование определенных областей ДНК может наследоваться, т. е. передаваться от родителей к следующим поколениям (Jones, 2001). Благодаря ряду скрещиваний ГМ-растения с его природной формой можно получить гибрид, у которого нет измененной ДНК, но метилирование сохраняется. Такой гибрид уже не будет считаться генетически модифицированным.

Насколько метилирование безопасно? Достаточно, ведь метильные группы присоединяются к ДНК совсем не в случайных местах. Поэтому, в отличие от традиционных методов селекции, результаты такого воздействия предсказуемы: мы можем заранее выбрать ген, кодирующий определенный белок, и просто заставить его замолчать. Но делать это нужно аккуратно, так как механизмы метилирования ДНК довольно сложны. Иначе в результате мы можем получить растение, подверженное болезням или преждевременному старению.
Иногда ДНК-метилирование, наоборот, является обязательным условием для начала работы гена. Ученые и это научились использовать: с помощью изменения метилирования ДНК можно увеличить активность генов, отвечающих за производство растением запасных белков. Например, регулируя метилирование, можно повысить содержание белков в зерне пшеницы, а путем обработки риса ингибитором метилирования (5-азацитидином) — получить растения с наследуемым признаком карликовости (Ванюшин, 2013).
Изначально Pixar помогал медикам
История Pixar началась в 1979 году в Сан-Франциско — в только что основанном отделе разработки производственной компании Lucasfilm’s Computer Division под шефством легендарного режиссера Джорджа Лукаса. Много позже Lucasfilm станет известной как одна из крупнейших кинематографических компаний мира (пока ее в 2012 году не поглотит Disney), но в 80-е она специализировалось на новых компьютерных технологиях для мира кино.

Эд Кэтмелл и Джон Лассетер в студии Lucasfilm. Фото pixar.com
Уже в то время Лукас понимал, что будущее за цифрой: компьютерной графикой и цифровыми системами редактирования. Чтобы дать жизнь новому подразделению, он много месяцев провел в поисках подходящего специалиста. Поиски увенчались успехом — отдел возглавил талантливый разработчик, специалист в области компьютерной графики Эд Кэтмелл, которого Лукас переманил из Нью-Йоркского технологического института.
Помимо того, что Кэтмелл был настоящим самородком и компьютерным гением, он был еще и преданным фанатом Disney и буквально грезил мультипликацией. Хотя до того момента, когда ему это пригодится, пройдет еще немало лет. Пока же отдел Кэтмелла с неменьшим энтузиазмом всерьез взялся за разработку мощного компьютера и софта, позволяющего заниматься высокотехнологичным моделированием и анимацией. Релиз итога многолетней работы команды Pixar Image Computer состоялся лишь в 1986 году.
В отличие от других компьютеров, программное обеспечение Pixar создавало трехмерные цветные изображения с высоким разрешением практически всего: от зданий и автомобилей до торнадо и пришельцев. Разработка нашла свое применение и за пределами мира кино: ПО Кэтмелла помогало медикам диагностировать заболевания по 3D-изображениям CAT-сканов и рентгеновских снимков и пригодилось метеорологам для получения изображений со спутников.
Работая над технической составляющей Lucasfilm, Эд Кэтмелл не расставался со своими творческими задумками: в 1983 году он приглашает в команду молодого художника-аниматора, выпускника Калифорнийского университета искусств (который был основан Уолтом Диснеем) Джона Лассетера в качестве дизайнера интерфейса. На базе разработок Кэтмелла Лассетер фактически создает первый в мире мультфильм, выполненный с помощью компьютерной графики, — короткометражную ленту «Приключения Андре и Пчелки Уолли».

Pixar Image Computer в музее студии Pixar. Фото pixar.com
«Когда я пришел, отдел разработки Lucasfilm был очень маленькой командой, но это были самые умные, самые удивительные компьютерные исследователи со всего мира. Они привели меня к работе над самой первой трехмерной компьютерной анимацией персонажа. Тогда я занимался разработкой вещей в «Диснее», но в то время компьютеры создавали только фоны, а персонажи по-прежнему анимировались вручную. Но Эд бросил мне вызов», — рассказывал Джон Лассетер в интервью The Daily Telegraph в 2015 году.
Дата презентации мультфильма, 1984 год, вошла во все учебники по мультипликации и графическому дизайну, технология стала прорывом для всей киноиндустрии, хотя хронометраж «Приключений Андре и Пчелки Уолли» составил всего 1,5 минуты. Фильм считается первым фильмом Pixar, хотя в реальности такой студии еще не существовало.
Поглощение The Walt Disney Company
В 2006 году Стив Джобс продает Pixar The Walt Disney Company за $7,4 млрд. Для бизнесмена это не было простым решением, сделке предшествовали непростые события в его жизни. В 1996 году Apple приобретает NeXT, компания переживает не лучшие времена, и Джобс возвращается на должность генерального директора, помогая «яблочному» бизнесу нащупать новые точки роста. Параллельно он отходит от операционного руководства Pixar. В 2003 году становится известно об ухудшающемся состоянии здоровья Джобса, и он окончательно решает снять с себя часть нагрузки.
По условиям сделки, Джобс не потерял место в совете директоров Pixar и получил 7% акций Disney, став крупнейшим акционером компании среди физлиц. Джон Лассетер был назначен на должность главного креативного директора Pixar и подразделения Disney Animation, а Эд Кэтмелл полноценно встал у руля студии. Одним из главных отступных требований Джобса, по настоянию партнеров, стало полное невмешательство Disney в творческие процессы Pixar и сохранение всей команды. Disney, судя по всему, держит обещание и сейчас: тандем продолжает выпускать анимационные полнометражки и собирать приличные кассы по всему миру. В новейшей истории Pixar выпустил 10 оскароносных фильмов, включая мультфильмы «Рататуй», «ВАЛЛ-И», «Вверх», «Головоломка» и «Тайна Коко».
The Walt Disney Company не раскрывает информацию отдельно по каждому из своих активов, в том числе и Pixar, однако косвенно можно судить о том, что студия приносит хороший процент прибыли головной компании. По данным Bloomberg, выручка Disney в 2018 году выросла на 7,8%, составив $59,4 млрд. Одним из самых прибыльных сегментов для компании традиционно стал прокат, здесь особенно отметились шесть полнометражных картин, одна из которых, «Суперсемейка 2», создавалась именно на базе Pixar.
P. S. Эд Кэтмелл в возрасте 73 лет по-прежнему находится в рядах топ-менеджмента Pixar. Джон Лассетер 8 июня 2018 года был вынужден покинуть Disney из-за громкого скандала. По данным The Washington Post, режиссер был обвинен в сексуальных домогательствах и непристойном поведении по отношению к подчиненным. В январе 2019 года стало известно, что Лассетер возглавил американскую продюсерскую компанию Skydance Media, работающую над производством фильмов с Paramount Pictures Corporation.
Предыдущие выпуски:
Интернет-газета «Реальное время»
Бизнес
Первый «Оскар» и колоссальные издержки
В течение еще 10 лет Pixar будет заниматься выпуском анимационных рекламных роликов крупнейших мировых брендов, неоднократно студия удостаивалась премий за свежие идеи в рекламе, но действительно тяготела к другому. Возможно, компания и сейчас бы латала дыры в бюджете за счет коммерческих видео, если бы не упорство и настойчивость Кэтмелла и Лассетера: они продолжали разрабатывать и выпускать короткометражные мультфильмы с оригинальным сюжетом. В 1986 году состоялся режиссерский дебют Джона Лассетера: в кинотеатрах Лос-Анджелеса был показан анимационный фильм под названием «Люксо-младший», всего через пару месяцев он был номинирован на «Оскар» (но награду все же не получил).

Эд Кэтмелл, 1989 год. Фото lawrencelevy.com
К слову, главный персонаж ленты — настольная лампа Люксо стала прототипом логотипа Pixar. Ровно через год студия получила свою первую (но далеко не последнюю) статуэтку «Оскар» — свет увидела короткометражка «Оловянная игрушка». Хотя Джобс все еще ставил во главу угла технологическую сущность компании, ему все же пришлось пересмотреть свое мнение и дать большую свободу подопечным. В Pixar начинают задумываться о создании полного метра… в партнерстве с The Walt Disney Company.
Параллельно с этим команда Pixar разрабатывает революционную графическую программу, которая позволяет графическим художникам создавать цветные текстуры для экранных 3D-объектов, RenderMan. Студия патентует разработку в 1987 году и вплоть до 1990-го выпускает расширения для нее. Лицензионные сборы RenderMan наконец начинают окупаться: программу включают в свои продукты ведущие производители ПО — IBM, Intel Corporation и Sun Microsystems. Pixar достигает выручки в $3,3 млн, но все еще не выходит на прибыль. В то время как другая компания Джобса, NeXT, процветала, Pixar в 1991 году пытался свести концы с концами. В феврале из Pixar было уволено 30 сотрудников.
Соматический Франкенштейн
Интересно то, что в мощной законодательной «обороне» против ГМО оказались бреши, появившиеся благодаря ряду парадоксов и допущений, которые на руку смелым селекционерам. Один из примеров — соматическая гибридизация. Другими словами, формирование новых форм растений путем комбинирования ядерных и других (митохондриальных и пластидных) генов при культивировании и слиянии обычных соматических клеток, составляющих ткань растения и не принимающих участия в половом размножении. Этот тип гибридизации растений достаточно широко распространен, при этом на территории ЕС такие соматические гибриды не считаются ГМО. Соответственно их оборот не подвергается строгому контролю.
Что же это за волшебный способ селекции? На первом этапе клетки растений двух разных видов (как правило, культурного и дикорастущего) обрабатывают специальными агентами, разрушающими клеточную оболочку, чтобы получить протопласты. Далее химическим или механическим способом провоцируют слипание и слияние протопластов, которые в дальнейшем восстанавливают общую клеточную оболочку. В результате из двух и более «родительских» клеток образуется новый живой организм — регенерант, или соматический гибрид.
Судьба родительских геномов при этом может быть различной. Два ядра могут синхронно делиться без слияния, образуя двуядерные дочерние клетки. Если же они сольются во время митотического деления, то в итоге получатся устойчивые одноядерные дочерние клетки, несущие смешанный генетический материал. Что касается внеядерного генома, то он тоже может быть получен как от одного родителя, так и быть смешанным. С помощью соматической гибридизации можно получать самые разные гибриды, включая такие, создание которых в принципе невозможно половым путем: например, гибриды, несущие цитоплазматические гены не от материнского растения, а от обоих родителей; «цибриды», содержащие ядро от одного из родителей, а цитоплазму от другого, и др.

Использование соматических клеток при гибридизации позволяет успешно работать с отдаленными, обычно нескрещиваемыми видами и полностью стерильными растениями. Иными словами, этот метод используют, если возникает необходимость преодолеть несовместимость культурных и дикорастущих видов. Таким способом можно получать межклассовые гибридные клеточные колонии: рис + соя, ячмень + табак и даже табак + мышь (Makonkawkeyoon, 1995)! Правда, большинство таких регенерантов сами размножаться уже не способны, а иногда и вовсе представляют собой скорее скопление клеток, чем полноценный организм.
Интересно, что, хотя метод соматической гибридизации влечет за собой значительную «перетасовку» генов, а его результаты очень непредсказуемы, он, тем не менее, разрешен для использования в сельском хозяйстве, в отличие от методов направленного мутагенеза. Как говорила Алиса в Стране чудес, «чем дальше, тем страньше».