Микробиологический контроль. Введение.
Микробиологический контроль консервированной продукции включает в себя:
- контроль микробиологических показателей сырья, полуфабрикатов, вспомогательных материалов, консервов перед стерилизацией;
- контроль рН заливки, консервированной продукции с регулируемой кислотностью (рН 3,8 — 4,2) перед стерилизацией или после стерилизации;
- контроль температурных параметров технологического процесса;
- посев консервов на промышленную стерильность;
- контроль стабильности консервированной продукции при термостатировании;
- контроль брака, выявленного в партии консервов при этикетировке продукции;
- контроль санитарного состояния тары, оборудования, личной гигиены сотрудников.
Содержание
- Введение
- Краткий исторический обзор развития микробиологии
-
Глава I. Краткие сведения об общей морфологии и физиологии микроорганизмов
- Бактерии
- Грибы
- Систематика микроорганизмов
- Процессы питания и дыхания у микроорганизмов
- Глава II. Ферменты и их значение для микроорганизмов
- Природа ферментов и механизм их действия
- Номенклатура и классификация ферментов
- Глава III. Микроорганизмы и среда
- Условия проявления активной жизнедеятельности микробов
- Влияние физических факторов на развитие микроорганизмов
- Влияние химических факторов на развитие микроорганизмов
- Влияние биологических факторов на развитие микроорганизмов
-
Глава IV. Важнейшие биохимические процессы, возбуждаемые микроорганизмами
- Спиртовое брожение
- Глицериновое брожение
- Молочнокислое брожение
- Маслянокислое брожение
- Брожение пектиновых веществ
- Разложение клетчатки
- Разложение жиров и высших жирных кислот
- Уксуснокислое брожение
- Лимоннокислое брожение
- Аммонификация белка (гниение)
- Значение микробиологического контроля на консервных заводах и организация микробиологических лабораторий
- Глава V. Аппаратура, приборы и посуда микробиологической лаборатории и методы стерилизации
- Методы уничтожения (стерилизации) микробов
- Приспособления и посуда для посевов микроорганизмов
- Термостат
-
Глава VI. Питательные среды и их приготовление
- Простые питательные среды
- Специальные питательные среды
- Элективные среды для выделения кишечной палочки
- Дифференциально-диагностические среды
- Молочные среды
- Среды для выращивания дрожжей и плесеней
- Использование сухих питательных сред
- Обращение с бактериальными культурами и методы посева на питательные среды
- Глава VII. Микроскоп и техника микроскопирования
- Устройство микроскопа и его назначение
- Техника микроскопирования
- Приготовление микроскопических препаратов
- Глава VIII. Микробиология консервного сырья
- Плоды и овощи
- Химический состав плодов и овощей
- Микробиология плодов и овощей
- Наиболее распространенные в консервном производстве виды порчи плодов и овощей и краткая характеристика их возбудителей
- Мероприятия по борьбе с болезнями плодов и овощей при хранении
- Мясо
- Рыба
-
Глава IX. Санитарно-бактериологический контроль производства баночных консервов
- Методы бактериологического исследования сырья и полуфабрикатов
- Выявление кишечной палочки, аэробов и анаэробов в консервном сырье
- Микробиологический контроль технологических операций
- Бактериологический контроль качества консервов перед стерилизацией
- Контроль вакуумирования и закатки банок
- Стерилизация консервов
- Микробиологический контроль вспомогательных материалов
- Остаточная микрофлора консервов
- Санитарно-бактериологические показатели готовых консервов
- Микробиологический бомбаж консервов
- Патогенные микроорганизмы, вызывающие отравление консервами
- Глава X. Санитарные анализы на производстве
- Производственное значение воды
- Санитарно-бактериологическое исследование воды
- Микробиологическое исследование воздуха
- Санитарно-бактериологическое исследование смывов с рук
- Санитарный контроль технологического оборудования, инвентаря, тары и рабочих мест
- Глава XI. Технологические особенности производства и источники микробиального загрязнения консервов
- Овощные натуральные консервы
- Овощные закусочные консервы
- Пюреобразные консервы для детского и диетического питания
- Томатопродукты
- Консервированные овощи и слабокислые маринады из овощей и фруктов
- Мясные и мясо-растительные консервы
- Консервированные обеденные блюда
- Рыбные консервы
- Квашеные и соленые овощи
- Заключение
Исследование воды для охлаждения банок
Для лаборатории консервного производства исследование воды для охлаждения должно рассматриваться как существенная обязательная процедура. Если вода повторно используется и хлорируется, необходимы регулярные определения как остаточного хлора, так и количества бактерий. Частота проведения таких анализов будет зависеть от типа завода и может быть установлена только опытным путем.
Определение содержания бактерий. При некоторых обстоятельствах желательно исследовать воду на специфические микроорганизмы. При контроле чистоты воды для охлаждения банок достаточно метода подсчета на чашке. При исследовании воды для питьевых целей большее значение придают подсчету микроорганизмов, выросших три 37°, чем выросших при 22°, так как первая группа относится к паразитическим типам, которая служит показателем загрязнения сточными водами или отбросами. Большинство микроорганизмов, обнаруживаемых при порче, вызванной негерметичностью тары, попадают в консервы из воды и почвы и растут лучше при 25°. Поэтому подсчет на чашках при этой температуре имеет большое значение, если это касается воды для охлаждения банок.
Образец воды должен быть взят из душа или из места втекания в тэнк, предназначенный для охлаждения. Во всех случаях воде нужно дать стечь в течение нескольких минут до отбора образца в стерильную склянку или бутылку. Если вода хлорировалась, рекомендуется добавить в бутылку до стерилизации небольшой кристалл гипосульфита натрия, чтобы удалить свободный хлор. Если вода очень загрязнена, ее разводят в отношении 1:1000 в стерильной воде. Если предполагается, что вода хорошего качества, достаточно приготовить только одно разведение 1:10. После полного перемешивания путем 25-кратного встряхивания вверх и вниз отбирают пипеткой по 1 мл от образца и от каждого разведения в две стерильные чашки Петри
В чашку наливают 10-15 мл стерильного питательного агара, охлажденного до 45°, или декcтрозо-триптонового агара, охлажденного до 45°, осторожно перемешивают быстрыми — взад и вперед, а также круговыми движениями. При этом чашки должны стоять на ровной поверхности
После застывания чашки выдерживают в термостате при 25° не менее 5 дней. Чашки, на которых выросло не более 300 колоний, отбираются для подсчета. Чашки, на которых меньше 30 колоний, не должны подсчитываться.
Если имеется заметное расхождение между двумя чашками любого разведения, правильность подсчета ставится под сомнение. Установленных стандартов на охлаждающую воду нет, но если микроорганизмов имеется меньше 100 на 1 мл, то это считается удовлетворительным. Маловероятно, чтобы использование воды такого качества давало заметную порчу, если только швы банок отвечают стандарту. Фирма, выпускающая реактив хлоротекс, прилагает карту окрашиваний, полученных при применении 5 мл реагента, растворенного в 50 мл воды. Оттенки цветов на карте соответствуют концентрациям хлора от 0,00001 до 0,0001%.
Определение содержания хлора. Содержание свободного хлора в воде для охлаждения может быть определено колориметрически.
Мясные консервы: источники микрофлоры
Мясные консервы обсеменяются микроорганизмами за счет микрофлоры сырья, используемого для консервирования, а также из различных источников в процессе его подготовки для закладки в банки, при закладке в банки и порционировании.
Сырье и его подготовка.
Мясные консервы
вырабатывают и мяса животных и субпродуктов, которые всегда в той или иной степени обсеменены различными сапрофитными микробами.ю
Мясные консервы портят:
- анаэробные клостридии,
- термофильные бациллы,
- токсигенные и патогенные микроорганизмы:
- палочка перфрингенс,
- токсигенный стафилококк,
- сальмонелла и др
Мясные консервы при изготовлении кроме мясного
сырья дополняются растительным (бобы, фасоль, горох и др.), которое может быть источником обсеменения продукта микроорганизмами. На поверхности гороха, фасоли и другого растительного сырья обычно обнаруживают десятки и сотни тысяч микробов. Основную микрофлору растительного сырья составляют почвенные спорообразующие микроорганизмы.
Следовательно, мясо и растительное сырье — это основные источники микрофлоры консервируемых продуктов,
поэтому при производстве консервов к мясному сырью предъявляют более высокие требования, чем при производстве колбас.
Мясные консервы вырабатывают из мяса и субпродуктов, полученные от здоровых, упитанных животных. Нельзя применять сырье, плохо обескровленное, загрязненное, дважды замороженное, условно годное.
Мясное и растительное сырье обсеменено микроорганизмами в основном с поверхности. Поэтому непосредственно перед переработкой его необходимо подвергнуть тщательной санитарной обработке (зачистке и мойке). При этом вода, используемая для мойки сырья, должна соответствовать требованиям ГОСТа на питьевую воду и не содержать спор анаэробных клостридии в 100 мл. При подготовке мясного сырья к закладке в банки, т. е. при разделке, обвалке и жиловке мяса, происходит его дальнейшее обсеменение микроорганизмами. Источниками обсеменения могут стать инструменты, обвалочные столы и другой инвентарь, тара, руки и спецодежда рабочих, воздух производственных помещений. Следовательно, степень обсеменения подготавливаемого сырья микроорганизмами находится в прямой зависимости от санитарно-гигиенических условий производства.
Закладка сырья и вспомогательных материалов в банки и порционирование.
Мясные консервы больше
всего обсеменяются в процессе закладки плотных составных частей продукта (мясо, растительное сырье, пряности), заливки жидких составных частей (бульон, соус) и доведения массы нетто до стандартной ( порционирование). При этом источниками обсеменения могут быть руки рабочих (при ручной раскладке) или оборудование (наполнительные машины), а также вспомогательные материалы (пряности, соль, сахар, бульонная добавка и др.), которые всегда содержат микроорганизмы.
|
сырье и вспомогательные |
микроорганизмы,обсеменяющие |
| Пряности( перец, лавровый лист, кориандр, гвоздика и др.) |
различные виды аэробных бацилл и анаэробных мезофильных и термофильных клостридии, сильно обсеменены микроорганизмами молотые пряности, обсемененность составляет десятки и сотни тысяч, а иногда и миллионы микробных клеток в 1 г |
| Соль и особенно сахар | обсеменены (до 80 %) разными спорообразующими микроорганизмами, например, мезофильными аэробными бациллами и анаэробными клостридиями. |
| Жир-сырец и топленый жир | содержат бесспоровые микроорганизмы итермоустойчивые спорыаэробных и анаэробных микроорганизмов |
| бульонная заливка | порообразующие термофильные микроорганизмы, попадающие в нее из трубопроводов бульоноварочных установок |
| консервная тара (банки) | различные кокковые бактерии, мезофильные аэробные бациллы и анаэробные клостридии, неспорообразую-щие гнилостные бактерии, плесени, дрожжи, актиномицеты и бактерии группы кишечных палочек. |
Статьи по этой тематике : Влияние остаточной микрофлоры на качество консервов Санитарно-гигиенические требования к производству консервов Микробиология шкур и кишок убойных животных Микрофлора кишечных продуктов Ветеринарно-санитарные требования к кожевенному и кишечному сырью
Комментарии читателей
|
||||
Контроль режима стерилизации консервов
Как основной процесс консервирования, предопределяющий качество и сохранность консервируемого продукта, стерилизация требует соответствующего контроля. В настоящее время для контроля за температурой и давлением внутри автоклава в процессе стерилизации пользуются измерительными приборами — термометрами и манометрами; в автоклавных отделениях монтируют терморегистрирующие приборы — термографы, записывающие температуру внутри автоклава при: стерилизации консервов. Неудобство термографов заключается в том, что> они только фиксируют, но не регулируют температуру в автоклаве.
В последнее время широкое применение получают терморегуляторы: конструкции Бабенкова, дающие возможность управлять процессом стерилизации консервов в автоклавах без регулируемого противодавления. В тех случаях, когда контроль режима стерилизации осуществляется с помощью термографов, проверку термограмм (бумажный круг или лента, на которой записана температура) ведет старший микробиолог. Он ежедневно просматривает термограммы и в случае нарушения режима стерилизации принимает меры к ликвидации нарушений.
При разработке новых режимов стерилизации, когда нужно измерить температуру в центре банки или определить скорость прогревания ее содержимого, пользуются термопарами (рис. 73). Термоэлектрический метод измерения температуры в центре банки является наиболее совершенным. Термопара — это две спаянные металлические пластинки из разных металлов, например из меди и константана, из нихрома и никелина и т.д. К концам каждой пластинки припаивают провода, которые подсоединяются к гальванометру. Пластинки и нижние концы проводов помещаются в автоклав. Для изоляции от греющей среды и предохранения от механических повреждений их предварительно укладывают в защитный кожух, например, в толстую резиновую трубку. Термопара может и не иметь пластинок, а непосредственно используются два спаянных на одном конце провода из меди и константана.
При нагревании места спая двух разных металлов возникает разность потенциалов, пропорциональная величине нагрева. При измерении температуры в центре банки при стерилизации спаянный конец термопары помещают в центр банки, а свободные концы проводов, выведенные из банки, подключают к гальванометру. Шкала гальванометра, регистрирующего возникающую при нагреве разность потенциалов, может быть градуирована непосредственно в градусах температуры. Наблюдая за перемещением стрелки гальванометра во время стерилизации и фиксируя температурный уровень во времени, строят кривые проникновения тепла в центр банки. По оси абсцисс откладывается время стерилизации, по оси ординат — температура.
Определение термоустойчивости микробов
Наиболее простой и в то же время достаточно точный метод определения термоустойчивости микробов (по В. Л. Омелянскому) состоит в том, что небольшое количество суспензии изучаемого микроорганизма в водном или солевом растворе подвергают действию желаемой температуры в запаянном капилляре короткой пипетки Пастера (рис. 72). Пипетки Пастера предварительно закрывают длинными (двойными) ватными пробками и стерилизуют сухим жаром. После стерилизации конец запаянного капилляра оттягивают на пламени горелки в тончайший волосок, конец которого обламывают стерильным пинцетом. Тотчас же засасывают в капилляр пипетки суспензию изучаемого микроба и капилляр вновь запаивают. Приготовив таким образом необходимое количество пипеток с исследуемым материалом, помещают их в отверстия асбестового картона, которым накрыта водяная баня, установленная на определенную температуру. Каждая пипетка выдерживается в водяной бане при заданной температуре назначенное время (5; 10; 15 мин и т.д.), по истечении которого последовательно вынимают каждую пипетку (лучше брать по две для проведения параллельного опыта), охлаждают капилляр в холодной воде и стерилизуют его конец. Стерилизовать капилляр можно погружением его в стакан со спиртом и эфиром. Простерилизовав капилляр, быстро подсушивают его над пламенем горелки, затем конец обламывают стерильным пинцетом и выдувают содержимое пипетки в стерильную чашку Петри. Посев заливают необходимой для изучаемого микроба питательной средой и выращивают в термостате при оптимальных температурах роста 24-48 ч. Наличие роста микробной культуры в чашке Петри будет свидетельствовать о степени термоустойчивости данного микроба.
В последние годы во ВНИИКОПе были разработаны усовершенствованные методы определения термоустойчивости микробов и их спор, более соответствующие условиям консервного производства.
Стерильный продукт (консервы) заражали специально приготовленной суспензией спор изучаемого микроба в воде или буферном растворе из расчета 10-100 тыс. спор на 1 г консервированного продукта. Зараженную (инокулированную) массу тщательным образом перемешивали и асептически с помощью шприца разливали в стерильные ампулы емкостью 1-2 мл. Ампулы запаивали и в специальных мешочках помещали в глицериновую баню при разных температурах (в °С) — 110; 115; 117; 125 — на определенные промежутки времени — на 1; 2; 3; 5 мин и т.д. После прогревания ампулы немедленно охлаждали в холодной воде и термостатировали 14 дней при 37°С. Если в ампулах наблюдался рост микробов (газообразование, помутнение среды, появление гнилостного запаха и пр.), то это свидетельствовало о стойкости микробных спор к данному температурному воздействию и его продолжительности. Из ампул, где роста не наблюдалось, содержимое переносили в пробирки со средой Китта-Тароцци и посев выращивали при 37 °С еще 48 ч. Отсутствие роста свидетельствовало о том, что время и температура нагревания являются летальными для спор изучаемого микроба.
В последнее время вместо ампул предложено использовать для определения термоустойчивости микробов капилляры из тонкостенных стеклянных трубок (толщина стенки 0,1 мм) длиной 7,5 см. В капилляр вводится суспензия изучаемого микроба и медь-константановая термопара. Прогрев исследуемой суспензии микробов в капиллярах осуществляется в термостатах ТС-24, заполненных специальным маслом или глицерином (жидкостями с точкой кипения выше 130°С). Новая методика дает возможность получить более четкие данные при исследовании закономерностей отмирания микробов при нагревании, так как исключает явление активации спор и «теплового шока» у микробной суспензии при достижении заданной температуры. С помощью этой методики можно изучать термоустойчивость микробов и их спор в температурном диапазоне 120-160°С.
При изучении термоустойчивости микробов и их спор в настоящее время определяют: 1) время, необходимое для полной гибели всех микробов и их спор; 2) время, необходимое для гибели 90% клеток; 3) температурный уровень (в °С), при котором число выживших клеток уменьшается в 10 раз. Эти данные необходимы при разработке режимов стерилизации.
Источники микробиальной обсемененности
В главе, излагающей основы тепловой стерилизации, отмечено чрезвычайно важное значение зависимости, существующей между количеством микроорганизмов-возбудителей порчи, присутствующих в пищевых продуктах, и степенью нагревания, необходимого для их уничтожения. Практический и лабораторный опыт учит, что для уничтожения большого количества микроорганизмов требуется более жесткий режим тепловой обработки, чем при низкой обсемененности продукта
Лишь у очень незначительного числа видов консервов органолептические качества не снижаются при нагревании в течение определенного периода, продолжительность которого зависит от вида продукта. Ввиду того, что нормальная тепловая обработка пищевых продуктов достаточна для обеспечения стерильности лишь в случае отсутствия избыточной обсемененности, подготовка продуктов для консервирования должна быть связана с мероприятиями, снижающими количество присутствующих микроорганизмов в продукте и предотвращающими их попадание в банку до стерилизации.
Опасность попадания микроорганизмов внутрь банки после стерилизации имеется лишь в случае нарушения герметичности шва. Возможна течь из швов и в процессе охлаждения; порча содержимого в этом случае может зависеть от степени чистоты охлаждающей воды с бактериологической точки зрения.
В качестве источников микробиального загрязнения консервов можно рассматривать четыре основные категории:
1. Сырье.
2. Оборудование, посуда и пр.
3. Тара.
4. Вода для охлаждения.
Различные методы исследования консервов
Разведение культуры. Кроме продуктов, консервированных теплом, консервщики выпускают различные продукты с добавлением пищевых кислот, соли и сахара в разных сочетаниях. В некоторых случаях продукты под соусом или маринады подвергаются умеренной тепловой обработке, но часто остаются нестерильными, особенно в тех случаях, когда не применяется нагревание. Основная задача — определить, какие из присутствующих микроорганизмов вызывают порчу. Обнаружение роста в питательной среде мало поможет в этом отношении, разве только укажет на наличие возможных возбудителей порчи. Метод, который найден пригодным, включает постепенное разведение продукта с соответствующей питательной средой. Например, салатный крем бывает загрязнен дрожжами или кислотоустойчивыми бактериями, поэтому нужно развести 5, 10, 20 и 50% крема суслом и выдерживать смесь при 25°. Если брожение обнаруживается в самом низшем разведении, то мало гарантии, что продукт будет противостоять порче. Если для того чтобы выявить брожение необходимо значительное разведение, можно сделать вывод, что продукт умеренно устойчив к порче. Одним из методов, пригодных для испытания, является следующий.
Соответствующие разведения продукта заражаются микроорганизмом, вызывающим порчу, и результаты периодических подсчетов жизнеспособных клеток в каждой смеси наносятся на миллиметровку. Из получаемых таким образом кривых можно судить о пригодности метода.
Нок описал метод для предсказания примерного процента банок консервированного горошка, которые будут кислыми после термостатирования при 55°.
Споры, вызывающие плоскокислую порчу подсчитываются в нестерилизованных банках. По уменьшению количества спор в процессе стерилизации, которое исчисляется в десятых долях к исходному количеству, судят об эффекте стерилизации. Метод Нока применяется следующим образом:
1. Из линии отбирается непростерилизованная банка и энергично встряхивается в течение 1 мин., после чего ее вскрывают и жидкость сливают. 50 мл этой жидкости затем добавляют к 50 мл расплавленного двойной крепости декстрозо-триптонового агара в бутылке емкостью 200 мл с завинчивающейся крышкой. Горячую смесь автоклавируют в течение 10 мин. при 115°, после чего ее разливают в четыре чашки. Количество спор обозначается буквой r.
2. На кривой рис. 27 находят t — время, соответствующее десятикратному снижению количества опор для данного процесса стерилизации, включая 42% этого времени, расходуемого на подъем температуры.
3. Подсчитывают 10-t Cr, где Cr означает количество спор в нестерилизованной банке. C равняется объему жидкости в банке, деленному на 50*(5/2)*10. Множитель вводится для спор, прилипших к горошинам, множитель 10 для перевода количества микроорганизмов, выживших после тепловой обработки, указанной в п. 1, в первоначальное количество.
4. По кривой на рис. 28 подсчитывают наибольший возможный процент зараженных банок после стерилизации.
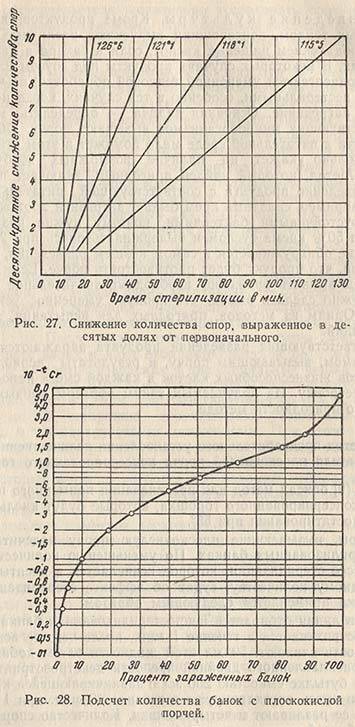
Нок обсуждает ошибки, допускаемые при работе по этому методу, тем не менее только на одном из 16 консервных заводов предполагаемые цифры плоскокислой порчи не совпадали с действительными; при этом вероятность предсказаний составляла 0,95 при инкубации 12 простерилизованных банок.
Бактериологическое исследование консервированной ветчины
Консервированная ветчина часто бывает нестерильна, поэтому в исследование этого продукта непременно включают выделение и классификацию обнаруживаемых микроорганизмов. Методика для исследования консервированной ветчины описана рядом исследователей. Техника открытия банок и отбора образцов подобна описанной ранее для других консервированных продуктов. Так как исследование направлено на идентификацию специфических микроорганизмов, включая патогенные, необходима специальная среда. Подробности можно найти в оригинальных работах.
По мнению Хоббса, патогенные микроорганизмы группы сальмонеллы и стафилококки, дающие положительную реакцию на коагуляцию, недопустимы в нормальной консервированной ветчине, даже если они выделены в небольших количествах.
Высококачественная ветчина должна быть свободна от вегетативных клеток. Допускаются только спорообразующие палочки в количестве меньше 1000 на 1 г.